pH / pH /
Qu'est-ce que c'est?
Le niveau de pH indique la concentration d’ions d’hydrogène d'une solution. Il permet de déterminer si cette solution est neutre (pH = 7), acide (pH < 7) ou basique (pH > 7).

Comment influence t-il la rivière et la biodiversité aquatique ?
Les organismes aquatiques fonctionnent de façon efficace à l'intérieur d'un écart de pH relativement restreint, en général entre 6 et 9. Un niveau de pH situé à l’extérieur de cet intervalle peut avoir de graves répercussions sur la biodiversité. Par exemple, des conditions acides ont un impact négatif sur les premiers stades de développement des insectes aquatiques et des poissons. De plus, elles créent un milieu propice à la dissolution des métaux lourds (par exemple le mercure, le plomb, le cadmium) issus du lessivage des sols et des sédiments. Les métaux lourds peuvent notamment causer des malformations chez les poissons immatures et perturber leur respiration.
Outre les niveaux extrêmes de pH, les organismes aquatiques supportent très mal les variations subites de pH.
Quels sont les facteurs qui influencent le pH ?
Le pH varie principalement selon les facteurs suivants :
- la géologie (type de sol) du bassin versant ;
- l’activité photosynthétique des plantes aquatiques et des algues (la photosynthèse provoque une augmentation du pH) ;
- les eaux de ruissellement contenant des abrasifs épandus sur les routes avec ou sans sous-produits d'exploitations agricoles ou minières ;
- les déversements industriels ou d'égouts.
Comment le mesure t-on ?
Il existe différentes techniques pour mesurer le pH. On peut se servir d’un appareil électronique muni d’une électrode, de papier indicateur ou d’un test colorimétrique.
Le pH s’exprime sur une échelle de 0 à 14. Cette échelle est logarithmique, c’est-à-dire qu’une augmentation d’une unité de pH correspond à un changement 10 fois plus grand. Par exemple, une solution à pH 8 est 10 fois plus basique qu’une solution à pH 7.
Unité utilisée : échelle de 0 à 14.
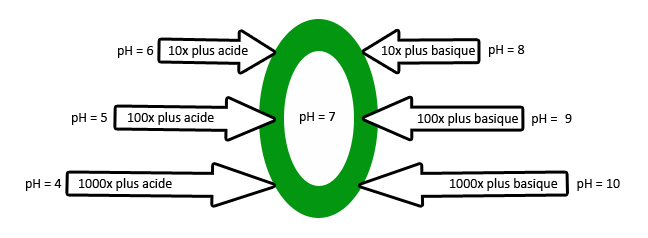
Échelle logarithmique du pH
Quelles sont les valeurs généralement observées ?
Le pH des cours d’eau se situe normalement entre 6 et 9. À l'intérieur de ces valeurs, le pH ne devrait pas varier de plus de 0,2 unité par rapport au pH naturel anticipé à une période déterminée.
Une expérience avec ça ?
Les réactions colorimétriques
Les tests colorimétriques utilisés pour mesurer le pH exploitent un principe chimique que l’on peut facilement reproduire en classe ou à la maison. Vous voulez tenter l’expérience! Suivez les étapes suivantes.
- Faites bouillir un chou rouge et récupérez le jus de cuisson. Un demi-litre est suffisant pour trois solutions à tester.
- Vous devrez aussi préparer vos solutions à tester, au minimum une acide, une neutre et une basique :
- pour la solution acide, vous pouvez prendre du jus de citron ou du vinaigre;
- pour la solution neutre, de l'eau ;
- pour la solution basique, du bicarbonate de soude ou de l’eau de Javel.
- Remplissez à moitié trois verres avec les solutions à tester. Si l’acidité des solutions est connue, vous pouvez aligner les verres par ordre d’acidité croissante pour faciliter l’interprétation.
- Ajoutez ensuite doucement le jus de chou rouge, environ la moitié du volume de la solution à tester.
- Mélangez le contenu des verres en changeant ou nettoyant votre cuillère entre chaque verre et observez les changements de couleur.

Interprétation :
Lorsque le jus de chou rouge est versé dans les solutions acides ou basiques, vous observez un changement de couleur. Les pigments du chou rouge réagissent au pH de la solution et prennent une coloration : rouge en milieu acide et jaune en milieu basique.
Dans le cas de solutions neutres, il n’y a pas de changement de couleur, la solution prend la couleur violette du jus de chou rouge.
Si vous le désirez, vous pouvez préparer plus d’échantillons pour tester différentes concentrations ou caractériser une solution mystère.
